PHOTOCHIMIE
La photochimie est l'étude de l'action de la lumière sur les réactions chimiques. D'une façon plus précise, elle regroupe les travaux dont la finalité est de déterminer la nature des états excités réactifs des molécules obtenues par absorption de la lumière, d'étudier les processus de désactivation de ces états, notamment ceux qui conduisent à des produits différents des réactifs irradiés et d'établir les mécanismes selon lesquels s'opèrent les réarrangements intra et intermoléculaires initiés par le rayonnement.
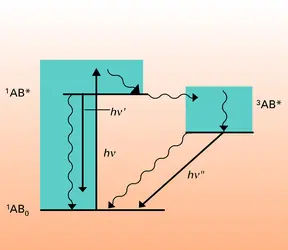
Par comparaison aux processus chimiques qui ont lieu dans l'obscurité et qui sont le fait de molécules en équilibre thermique avec leur environnement, la photochimie est le domaine d'étude d'un milieu réactionnel dans lequel des molécules d'une espèce donnée se trouvent sélectivement portées dans un état excité métastable riche en énergie, et qui ne pourrait être obtenu qu'en chauffant le mélange à des températures très élevées sans distinction d'espèces possible.
Dans certains cas, l'action de la lumière peut être assimilée à celle d'un catalyseur qui facilite une réaction dont l'énergie d'activation est élevée. C'est ce qu'on observe en irradiant un mélange d'hydrogène et de chlore qui réagit explosivement pour donner le chlorure d'hydrogène (HCl). Dans d'autres cas, la lumière est indispensable au déroulement de la réaction qui n'aurait pas lieu sans apport d'énergie ; la transformation de l'oxygène en ozone en est un exemple.
En outre, les molécules excitées peuvent souvent être considérées comme de nouvelles espèces chimiques, car leur géométrie et leur répartition électronique sont presque toujours différentes de celles des molécules non irradiées que l'on dit être dans leur état fondamental. Un exemple illustrant bien ce cas est celui de l'éthylène et de ses dérivés comme le dichloréthylène dont les molécules sont planes à l'état fondamental et non planes à l'état excité, les plans des deux groupements H − C − Cl faisant un angle de 900 entre eux.
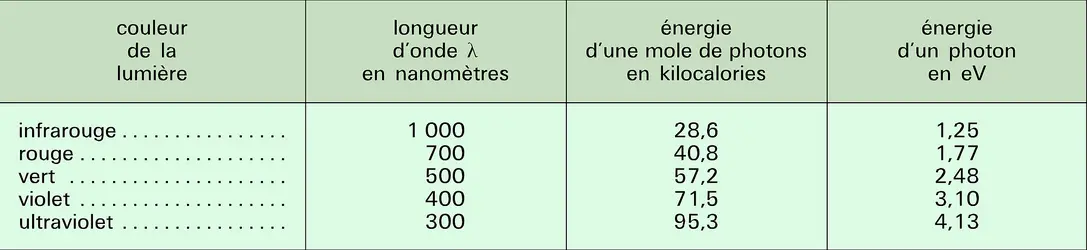
Les radiations actives en photochimie sont essentiellement les rayonnements électromagnétiques dans le domaine du visible et de l'ultraviolet. Depuis quelques années, on assiste à un élargissement du domaine d'action spectrale, d'une part vers les courtes longueurs d'onde de l'ultraviolet que fournissent les lasers à excimères et l'ultraviolet sous vide et d'autre part vers les grandes longueurs d'ondes de l'infrarouge grâce aux lasers à CO2.
Historique
Une légende rapporte qu'Alexandre le Grand avait muni ses soldats de bracelets en tissu imprégné d'une substance qui changeait de couleur selon l'heure, sous l'influence de la lumière du soleil. Mais, bien que l'on sache depuis longtemps que la lumière peut provoquer des transformations chimiques, les études quantitatives et systématiques n'ont été entreprises que depuis le milieu du xixe siècle.
Le lien entre la lumière absorbée et l'effet chimique qui en résulte a été tout d'abord clairement perçu, à partir de considérations théoriques, par T. von Grotthuss en 1817 et redécouvert, en 1841, par J. W. Draper, à la suite de ses expériences sur la combinaison de l'hydrogène avec le chlore. La loi énoncée alors, qui porte le nom de Grotthuss-Draper, dit que seules les radiations absorbées par les espèces chimiques peuvent provoquer une réaction photochimique.
On chercha alors pendant longtemps à relier l'avancement de la réaction photochimique à la quantité d'énergie absorbée, mesurée en ergs, en calories, etc., mais aucune relation simple ne put être trouvée avant l'introduction des quanta en physique. À la suite des travaux d'Einstein (1905-1912) et de[...]
La suite de cet article est accessible aux abonnés
- Des contenus variés, complets et fiables
- Accessible sur tous les écrans
- Pas de publicité
Déjà abonné ? Se connecter
Écrit par
- Jacques JOUSSOT-DUBIEN : docteur ès sciences, professeur, directeur de l'École nationale supérieure de chimie et de physique de Bordeaux.
Classification
Médias
Autres références
-
AÉRONOMIE
- Écrit par Gaston KOCKARTS
- 4 158 mots
- 11 médias
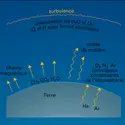
Commele rayonnement solaire est capable de photodissocier et d'ioniser certains constituants atmosphériques, il est évident que les produits de ces processus peuvent réagir chimiquement avec d'autres composés et donner naissance à toute une chimie aéronomique qui est parfois difficile à réaliser au... -
ATMOSPHÈRE - Chimie
- Écrit par Marcel NICOLET
- 3 554 mots
- 5 médias
Il convient tout d'abord de séparer l'action de la radiation solaire ultraviolette en deux domaines distincts correspondant respectivement à la photodissociation et à la photo-ionisation des constituants de l'atmosphère. Le domaine spectral de longueurs d'onde inférieures à 100 nm est lié à l'ionisation... -
CELLULE - L'organisation
- Écrit par Pierre FAVARD
- 11 031 mots
- 15 médias
...chaîne sont des réactions photochimiques qui fournissent l'énergie nécessaire au transport, car celui-ci ne peut se faire spontanément. Chaque réaction photochimique met en jeu une molécule de chlorophylle piège qui est excitée par l'énergie lumineuse qui est collectée par une antenne formée de molécules... -
CHIMIE - Histoire
- Écrit par Élisabeth GORDON , Jacques GUILLERME et Raymond MAUREL
- 11 189 mots
- 7 médias
...réactions induites par des ions lourds accélérés ; ils ont mis au point des méthodes performantes permettant de doser certains éléments à l'état de trace. Les photochimistes, qui s'intéressent aux interactions entre le photon et la matière, ouvrent l'accès à la connaissance de la structure et des états excités... - Afficher les 24 références